начало https://nobel-group.by/2020/02/15/hloraty-i-drugie-oksihlornye-zagryazniteli-v-molochnoj-produktsii-chast-1/
часть 2 https://nobel-group.by/2020/02/15/hloraty-i-drugie-oksihlornye-zagryazniteli-v-molochnoj-produktsii-chast-2/
часть 3 https://nobel-group.by/2020/02/15/hloraty-i-drugie-oksihlornye-zagryazniteli-v-molochnoj-produktsii-chast-3/
часть 4 https://nobel-group.by/2020/02/15/hloraty-i-drugie-oksihlornye-zagryazniteli-v-molochnoj-produktsii-chast-4/
Нормативное регулирование количества оксихлорных побочных продуктов
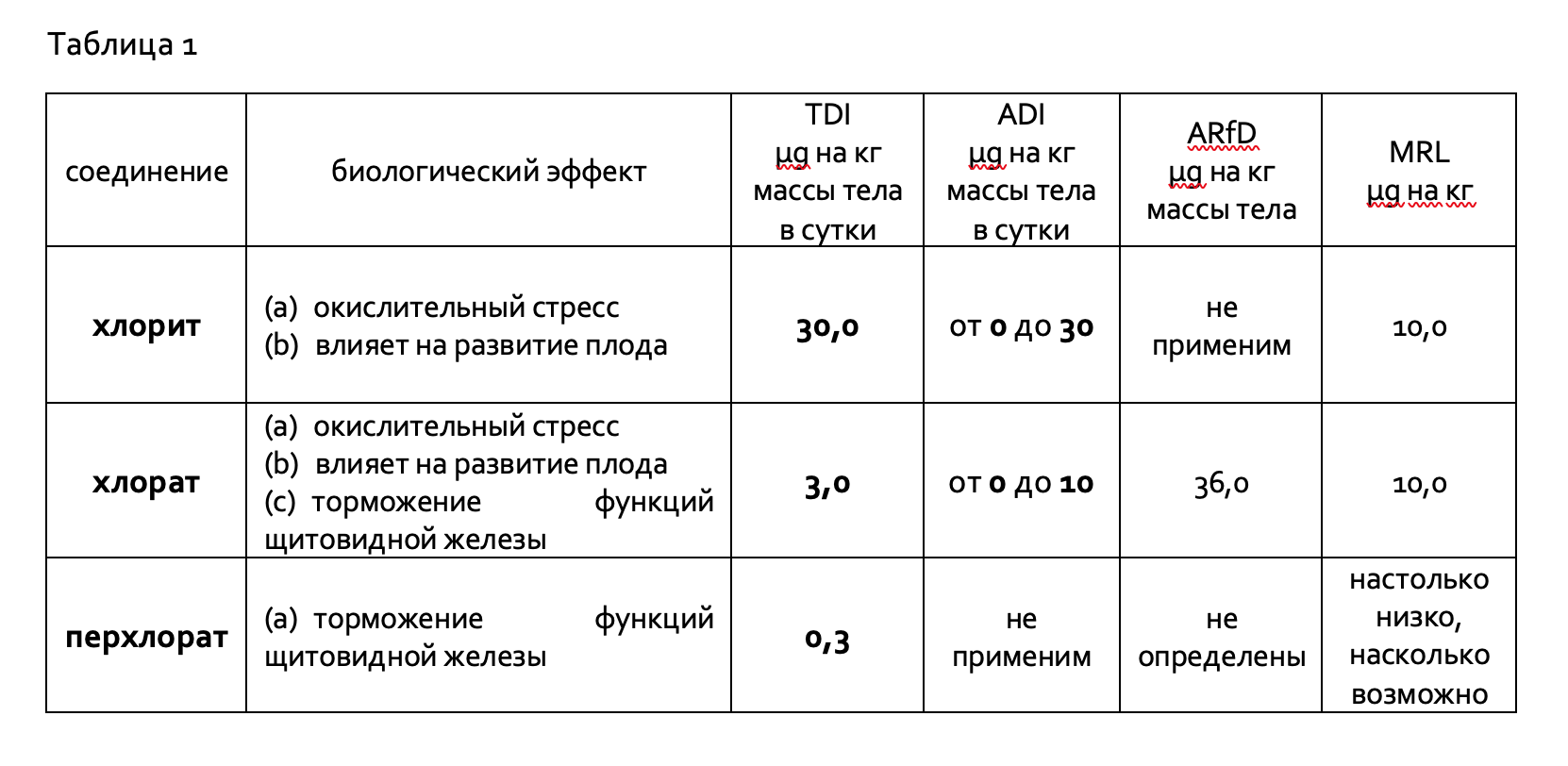
Максимальный остаточный уровень (MRL) – это максимальная концентрация вещества, определённая Комиссией Codex Alimentarius, и законодательно разрешенная в пищевых продуктах и кормах для животных. Такие ограничения являются критически важными, так как эти правила защищают потребителя от рисков неблагоприятных последствий для здоровья, связанных с потреблением таких побочных продуктов с пищей. Процессы очистки с использованием хлорсодержащих средств считаются основным путем, по которым оксихлорные побочные продукты попадают в пищу.
В исследование, проведенном в 2013 году немецким органом по контролю пищевых продуктов Chemisches und Veterinäruntersuchungsamt (CVUA) Штутгарта, определяли уровни контаминации пищевых продуктов, продаваемых в Германии, хлоратом. Было обнаружено, что уровни хлората выше нормативных пределов (> 10 мкг/кг) в 24,5 % отобранных проб со средним уровнем хлората для всех проб 22 мкг/кг. В отчете этого исследования были высказаны предположения о различных источниках загрязнения хлоратом, в том числе об использовании хлорированной воды, что впоследствии привело к тому, что ряд продуктов был изъят с рынка из-за уровней содержания хлората выше стандартного MRL в 10 мкг/кг. Следует отметить, что руководство WHO по хлорату в питьевой воде устанавливает уровень 700 мкг/дм3, что намного выше нормативных показателей, установленных для пищевых продуктов. Такая разница нормативов может оказать существенное влияние на уровень хлората в молочных продуктах, которые необходимо повторно гидратировать перед употреблением, например, таких как молочные смеси для детского питания или порошки пищевых высокопитательных белков.
TDI на уровне 0,3 мкг/ кг/сутки для людей был установлен Группой по загрязнителям в пищевой цепи (CONTAM) с использованием контрольного предела достоверности дозы (BMDL50), установленного для ингибирования перхлоратом поглощения йода щитовидной железой и с учетом фактора неопределенности для контрольной точки. Далее можно рассчитать TDI для хлората, применяя коэффициент экстраполяции для учета разницы в эффективности между химическими веществами. Используя коэффициент экстраполяции 10, TDI для хлората был рассчитан как 3 мкг/кг/день (2015 г.), что более чем в три раза ниже, чем допустимая норма суточного потребления (ADI), установленный ранее WHO.
Оценка рисков
Использование хлорсодержащих средств при очистке и дезинфекции оборудования молочных производств может привести к накоплению оксихлорных побочных продуктов в готовой продукции. Однако важно учитывать взаимосвязь между достижением необходимого уровня производственной санитарии и гигиены и, возможностью загрязнения продукта побочными оксихлорными продуктами. Оценка рисков должна быть завершена, чтобы полностью понять указанную взаимосвязь, оценить риски, особенно риски, связанные с неправильными режимами очистки, приводящие к контаминации продукции и последующего негативного воздействия на здоровье покупателей.
Потенциальные риски бактериологического загрязнения молока присутствуют уже на уровне молоко-товарных ферм и связаны с практиками, применяемыми в ходе производственных процессов. Подход и степень контроля над этими факторами варьируются от фермы к ферме, поэтому количество используемых моющих средств и соблюдение протоколов очистки могут варьироваться. В процессе промышленной переработки молоко пастеризуется, что снижает количество патогенов. На сегодняшний день не проведены тщательные исследований влияния практик промышленной переработки на загрязнение молочных продуктов хлоратом.
Исследование рынка, проведенное в 2014 году Chemisches und Veterinaeruntersuchungsamt (CVUA), показало, что уровень хлоратов в пищевых продуктах был проблемой рынка Германии. CVUA обнаружил, что 24,5 % проанализированных образцов были выше разрешенного MRL. Хотя такой уровень не был серьезной проблемой для большинства потребителей, так как потребление продуктов, загрязненных хлоратом, не превысило бы TDI. Однако обнаруженные уровни загрязнения хлоратом могут быть проблемой для детей в возрастных категориях с дефицитом йода или для взрослых с генетической предрасположенностью к гипотиреозу.
Полезные аспекты хлорных дезинфицирующих средств, применяемых в пищевой промышленности, снижают риски потребителей, связанные с болезнями пищевого происхождения, обеспечивая микробиологическую безопасность продуктов питания, однако существует необходимость более детального понимания проблемы контаминации пищевых продуктов побочными продуктами, образующимися в результате использования хлорсодержащих средств.
Методы удаления оксихлорных контаминантов
Разработка технологии удаления или уменьшения хлоратов является достаточно серьезной проблему для такого сложно структурированного продукта как молоко.
Удаление оксихлорных контаминантов
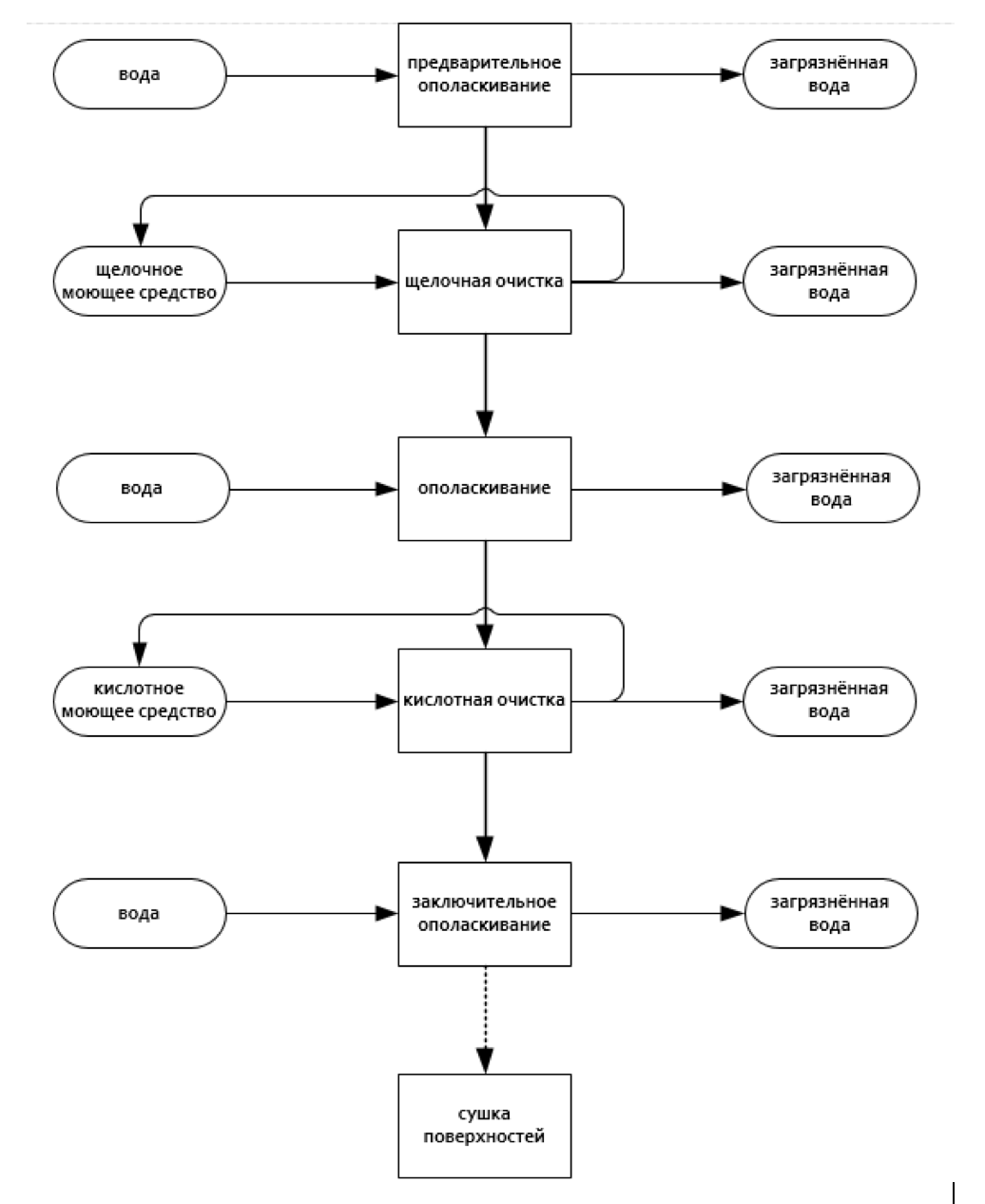
В сложных пищевых процессах, качество которых в значительной степени зависит от многоэтапных процедур CIP-очистки для обеспечения надлежащего гигиенического состояния оборудования, всегда существует риск загрязнения последующего пищевого продукта химическими контаминантами. Тем не менее, существует возможность разработки и внедрения методов удаления или восстановления, чтобы исключить такие контаминанты в растворах из продуктов в жидкой товарной форме, чтобы обеспечить их соответствие самым высоким стандартам безопасности пищевых продуктов.
Методы физического удаления не разрушают оксихлорные соединения и, следовательно, создают последующую потребность в удалении как оксихлорных соединений, так и других потоков отходов, образующихся в процессе. Кроме того, эти методы часто страдают от недостаточной селективности, так как наряду с оксихлорными соединениями они могут удалять большие количества растворенных солей, присутствие которых может быть желательным в структуре состава продукта.
Мембранное разделение селективно фракционирует вещества раствора через отверстия мембраны, разрушая её однородную непририрывность. Селективность мембран зависит от размера отверстий и приложенной силы. Мембранные процессы, такие как нанофильтрация и обратный осмос, эффективны при удалении оксихлорных соединений из воды, демонстрируя удаление более 80 % перхлората в растворе без его химического превращения. Тем не менее, использование мембран для удаления оксихлорированных веществ еще не было исследовано для молочной матрицы.
Среди методов удаления перхлората при очистке воды ионный обмен считается наиболее широко используемым методом удаления перхлората. С помощью этой техники перхлорат заменяется анионом, обычно хлоридом. Раствор протекает через смолу, содержащую высокие концентрации связанного иона. Относительная разница в концентрации каждого иона в смоле способствует обмену ионами и выделению обменного иона в раствор, в то время как целевые ионы остаются связанными со смолой. В конце концов, смола достигает равновесной концентрации, при которой она насыщается ионами, и затем смола требует регенерации. При обработке воды ионообменные смолы являются наиболее рациональным методом удаления перхлората на уровне <50 мкг/кг. Однако, ионный обмен видимо экономически нецелесообразен из-за высокой стоимости и необходимости утилизации солевых растворов. Также вероятно снижение адсорбционной способности смолы по перхлорату, когда другие вещества присутствуют в растворе.
Адсорбция — это адгезия молекул газа, жидкости или твердых веществ, находящихся в растворе растворе, к поверхности. Молекулы или атомы, которые адсорбируются (адсорбат), создают тонкую пленку на адсорбенте. Наиболее распространенные сорберы, используемые при удалении оксихлорированных веществ, представляют собой гранулированный активированный уголь (GAC). Эффективная адсорбция перхлората в GAC позволила использовать его как катализатор для гидрирования-восстановления перхлората и применить как технологию очистки воды в некоторых молочных установках.
Различные методы для удаления органических контаминатов из воды, например, таких как хлороформ, включают обратный осмос, ионный обмен, коагуляцию, осаждение, каталитическое восстановление, электродиализ и адсорбцию. Но, удаление оксихлорированных веществ и их предшественников коагуляцией с использованием органических полимеров не эффективно. Исследование альтернативных методов продемонстрировало, что адсорбционные процессы достаточно эффективны для удаления оксихлорированных веществ, что привело к использованию гранулированного и порошкообразного активированного угля.
Восстановление оксихлорных побочных продуктов
Электрохимическое восстановление разновидностей оксихлорированных веществ представляет значительный интерес, так как такие процессы технологичны, имеют низкое воздействие на окружающую среду и не используют токсичные растворители. Были проведены многочисленные исследования, связанные с восстановлением перхлората электрохимическими методами. Разработанный процесс электродиалитического ассистированного каталитического восстановления (EDACR) продемонстрировал 88 % удаление перхлората при катализе титаном (IV). В целом, EDACR включает в себя многоэтапную систему восстановления, включающую перенос, накопление и восстановление перхлората с последующим восстановлением хлоридов. Успешно продемонстрировано активированное углеродное волокно, легированное Pd / Pt-N (Pd / Pt-NACF), которое интегрировало адсорбцию и электрокаталитическое разложение перхлората путем эффективного электро-восстановления его в хлорид с помощью реакций гидродезоксигенирования, как показано ниже:
2Pd/Pt – H* + ClO4— ➔ 2Pd/Pt + ClO3— + H2O
2Pd/Pt – H* + ClO3— ➔ 2Pd/Pt + ClO2— + H2O
4Pd/Pt – H* + ClO2— ➔ 4Pd/Pt + Cl— + 2H2O
Превращение перхлората в хлорат является термодинамическим процессом, поскольку внутренняя энергия хлората ниже, чем у перхлората. Тем не менее, скорость реакции контролируется кинетическим барьером высокой энергии активации переходного состояния, который снижается с помощью катализа. Было отмечено, что в реакционной системе не было обнаружено никаких видов хлората или хлорита. Это означает, что кинетическая стабильность хлората и хлорита намного меньше, чем у перхлората, и они будут полностью восстановлены в хлорид после образования.
Биологически обусловленное сокращение (пер)хлората наблюдалось в различных средах и было связано с наличием диссимиляционных (пер)хлоратредуцирующих бактерий (DPRB), из которых многие штаммы были выделены и идентифицированы в последние годы. Метаболическая способность и повсеместное распространение этих микроорганизмов вызвали интерес к естественному восстановлению оксихлорированных веществ. DPRB способны восстанавливать оксихлорированные вещества и продуцировать безвредные хлорид-ионы, и, таким образом, были определены в качестве элемента потенциально возможного метода восстановления загрязнения оксихлорированных веществ.
DRPB были филогенетически отнесены к протеобактериям. Возможно, что их способность способны восстанавливать оксихлорированные вещества произошла от общего предка внутри Proteobacteria и была потеряна у нескольких родов, но другие теории предполагают, что это недавняя горизонтальная мутация. Последняя теория подтверждается отсутствием филогенетической синтении между генами рРНК 16s и хлорит дисмутазой (cld), существенным геном в цикле восстановления (пер)хлората.Путь реакции для восстановления перхлората до хлорида включает хлорат и хлорит в качестве промежуточных соединений:
ClO4— ➔ ClO3— ➔ ClO2— ➔ Cl— + O2
Этот путь восстановления включает ферменты (пер)хлорат редуктазу для восстановления форм +5 и +7 до хлорита, который подвергается диспропорционированию в хлорид и кислород при помощи хлорит дисмутазы.
Этот экологически чистый метод удаления оксихлорированных веществ, однако, он имеет низкую кинетику и чувствителен к температуре и pH. Однако этот метод может быть включен в процесс регенерацию смол. Было показано, что сшитую амином магнитную биополимерную смолу (AM-биополимер) после адсорбции можно подвергнуть микробной обработки, чтобы уменьшить концентрацию перхлоратов на поверхности смолы. На этом этапе одновременно шла регенерация смолы и удаление перхлората путём восстановления до хлорида и кислорода.
Новейшей технологией очистки воды и сточных вод является использование мембранного биопленочного реактора (MBfR), которые подают газообразный субстрат в биопленку, сформированную на внешней стороне мембраны. MBfR на основе водорода используется для удаления широкого спектра неорганических окисленных загрязнений. Было продемонстрировано, что широкий спектр химических веществ, в том числе хлорированные контаминанты, например, перхлораты, хлораты, хлориты и дихлорметан, могут быть эффективно восстановлены гидрогенотрофной биопленкой с использованием акцепторов электронов, таких как нитраты или кислород. MBfR на основе метана также могут использоваться для восстановления перхлората и могут быть экономически выгодными, так как метан относительно дёшев.
Вывод
В настоящее время признано, что использование средств для очистки и дезинфекции на основе хлора в процессах CIP не является оптимальным с учётом рисков образования большого количества хлорированных контаминантов. Однако риски, связанные с возможной контаминацией описанными вредными веществами готовой продукции, можно преодолеть путем ясного понимания химических процессов, ведущих к их появлению, и выработки мер, необходимых для минимизации их внедрения в цепочку переработки молока, начиная с уровня фермы. Чтобы обеспечить безопасность молочной продукции во время её промышленного производства необходимо проводить тщательный мониторинг моющих и дезинфицирующих средств с целью минимизировать загрязнение хлорированными побочными продуктами и, следовательно, повысить безопасность потребителей.