С согласия автора публикуем главу III из книги А. Н. Полякова «Краткий очерк истории медицинских масок«, посвященную проблеме эффективности использования масок, а также медицинским и социальным проблемам, связанным с их использованием.




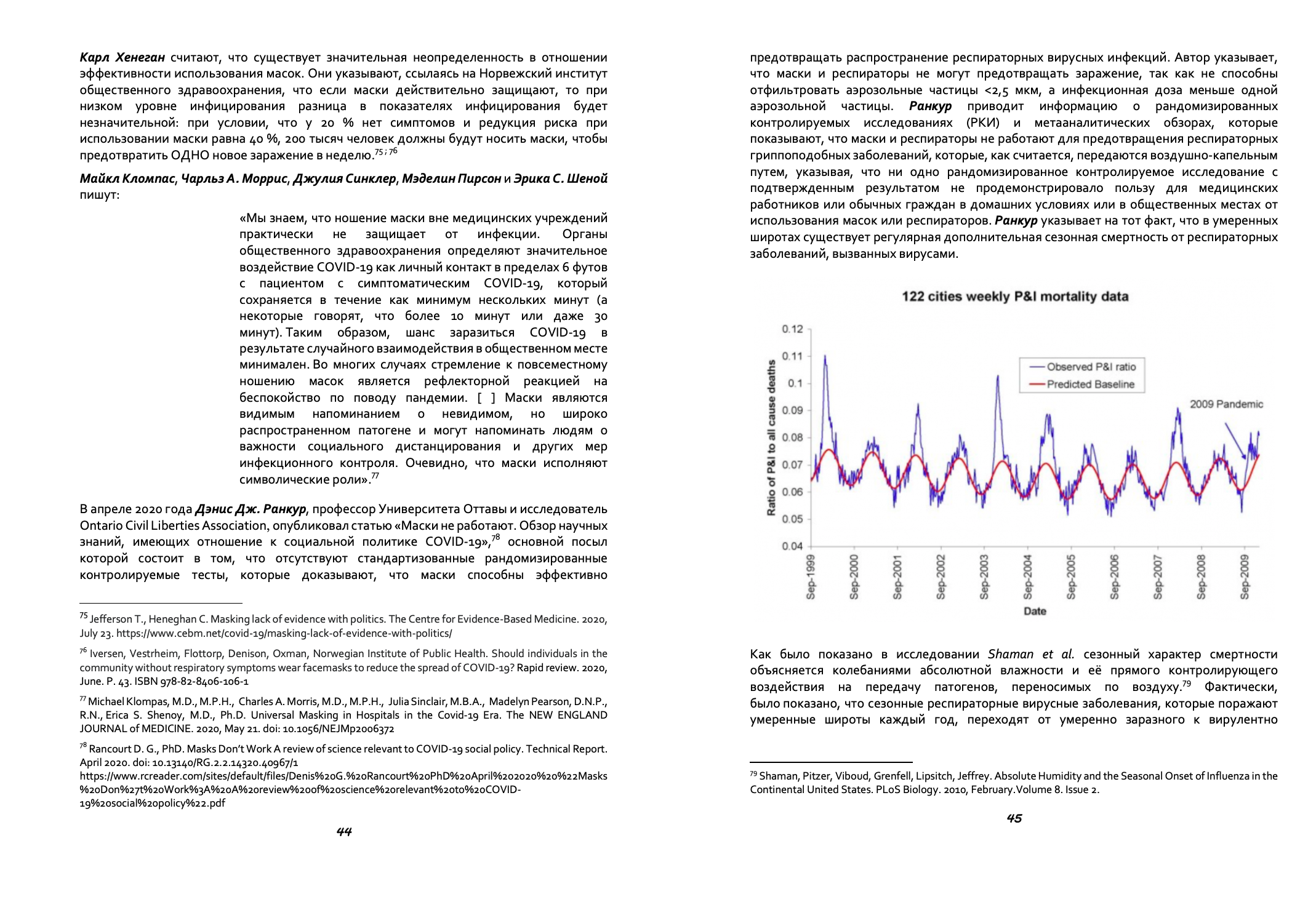






С согласия автора публикуем главу III из книги А. Н. Полякова «Краткий очерк истории медицинских масок«, посвященную проблеме эффективности использования масок, а также медицинским и социальным проблемам, связанным с их использованием.











Противоэпидемическая маска возникла в контексте эпидемии маньчжурской чумы 1910 – 1911 годов как симукляр «научно обоснованной борьбы» с невидимыми силами экзистенциального риска, имитируя «последний барьер» между человеком и «вирусами-убийцами».





Поляков А. Н.
Краткий очерк истории медицинских масок
– Almaty: nobel group publishing house, 2021. – 57 с., илл.
УДК 614.442
ББК 5г
После начала вспышки респираторной инфекции, соотносимой с вирусом SARS-CoV-2, из-за отсутствия компетенций и понимания как механизмов распространения инфекционных заболеваний, так и знания технологий, которые могут эффективно предотвращать распространение патогенов, начали использоваться устройства, бессмысленность и неэффективность которых очевидна любому специалисту. Одним из таких устройств является дезинфекция с использованием так называемых «дезинфекционных туннелей». Следует отметить, что WHO и FDA сразу указали на то, что нет никаких научных данных подтверждающих то, что указанные устройства способны хоть каким-то образом влиять на снижение уровня заражений и на то, что использование этих устройств может быть опасным. Приведенные ниже материал содержит тезисы небольшой аналитической записки, подготовленной 5 апреля 2020 года по просьбе одного государственного ведомства санитарно-эпидемиологического надзора.
Эффективность химической дезинфекции определяется:
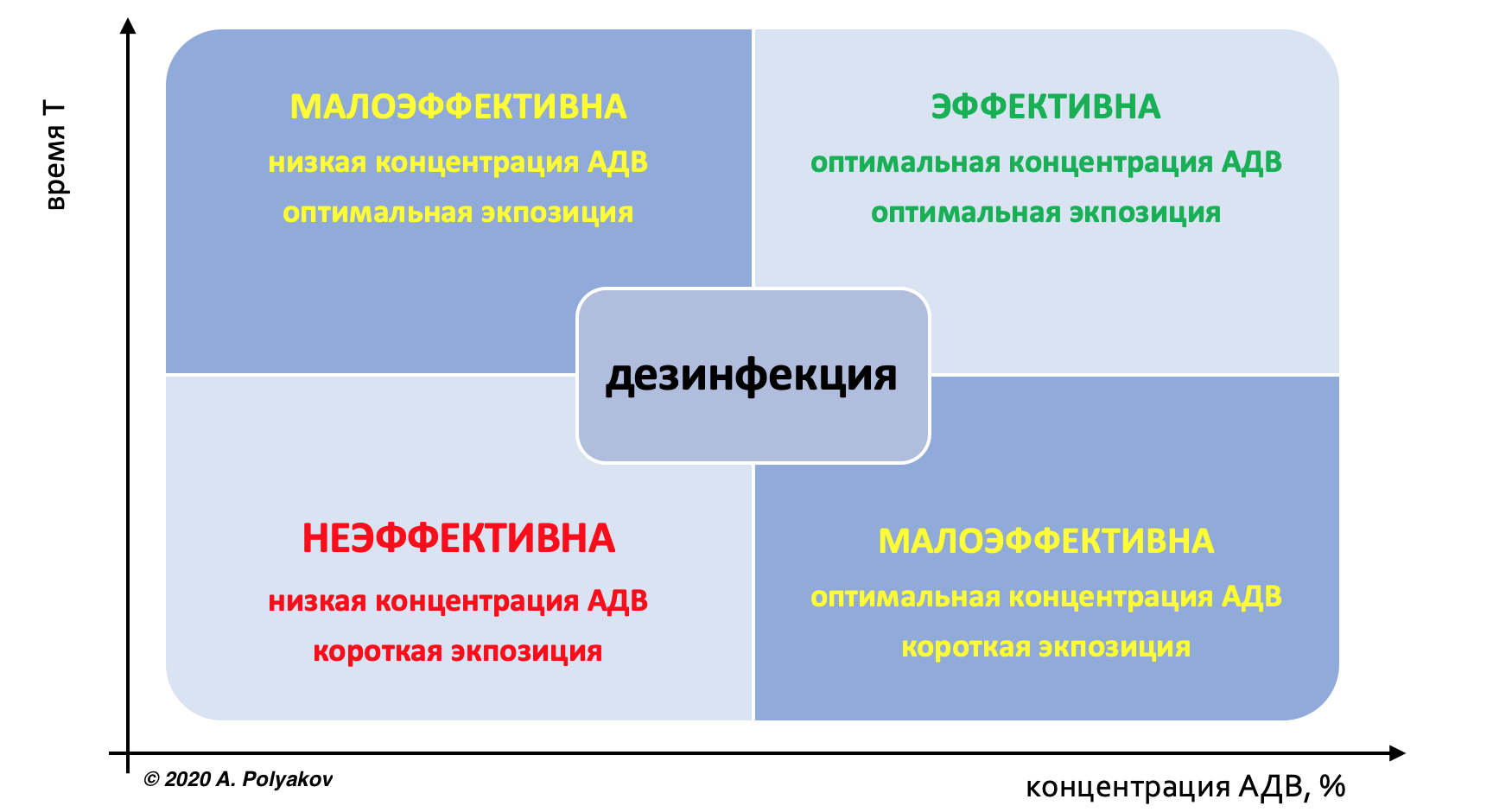
По просьбе одного из клиентов был проведен анализ соответствия антисептического средства условиям технического задания. Ниже приведена аналитическая часть экспертизы.
Спирты являются эффективными противомикробными средствами, наиболее широко используются этиловый спирт, изопропиловый спирт (изопропанол) и н-пропанол, который считается предпочтительным в EU [1]. Спирты обладают быстрым антимикробным действием широкого спектра против вегетативных бактерий (включая микобактерии), вирусов и грибов, не обладают спороцидным действием, но ингибируют споруляцию и прорастание спор [2]. Из-за отсутствия спороцидной активности спирты не рекомендуются для стерилизации, но широко используются как для дезинфекции твердых поверхностей, так и для антисептики кожи. Многие спиртовые дезинфектанты содержат незначительные количества других биоцидов, которые остаются на коже после испарения спирта, или вспомогательные вещества (включая смягчающие вещества), которые сокращают время испарения спирта и могут значительно повысить эффективность продукта [3]. Считается, что изопропиловый спирт несколько более эффективен против бактерий [4], а этиловый спирт более эффективен против вирусов [5]. Однако следует отметить, что такие эффекты зависят как от концентрации спирта, так и от тестового микроорганизма, например, изопропиловый спирт обладает более высокими липофильными свойствами, чем этиловый спирт, и менее активен против гидрофильных вирусов (например, полиовируса). Как правило, антимикробная активность спиртов значительно и нелинейно снижается в концентрациях ниже 50 %, поэтому оптимальным является содержание спиртов в составе продукта в диапазоне от 60 до 90 %.
Научного консенсуса о специфическом механизме действия спиртов нет, но, исходя из повышенной эффективности спиртов в присутствии воды, считается, что они вызывают повреждение клеточных мембран и быструю денатурацию белков с нарушением метаболизма и последующий лизис клеток [6], что подтверждается сообщениями исследователей о денатурации дегидрогеназы Escherichia coli [7] и увеличенной лаг-фазе Enterobacter aerogenes, предположительно из-за ингибирования метаболизма, необходимого для быстрого деления клеток [8].
Из научной литературы известно, что н-пропиловый спирт более эффективен, чем изопропиловый спирт (nPA — 3.12 % против iPA — 6.25 %), для уничтожения метициллинрезистентного золотистого стафилококка (MSSA) [9].
Соединения четвертичного аммония (ЧАС), являются наиболее эффективными дезинфицирующими активно-действующими веществами из группы КПАВ [10]. ЧАС используют для множества клинических целей (например, для предоперационной дезинфекции неповрежденной кожи, нанесения на слизистые оболочки и дезинфекции некритических поверхностей). Помимо антимикробных свойств, ЧАС также отлично подходят для очистки и дезодорации твердых поверхностей.
Известно, что ЧАС являются мембранно-активными агентами [11], преимущественно повреждающими цитоплазматическую мембрану бактерий или плазматическую мембрану грибов. Сэлтон [12] предложил следующую последовательность событий с микроорганизмами, подвергнутыми воздействию катионных агентов: (i) адсорбция и проникновение агента в клеточную стенку; (ii) реакция с цитоплазматической мембраной (липидом или белком) с последующей дезорганизацией мембраны; (iii) утечка внутриклеточного низкомолекулярного материала; (iv) деградация белков и нуклеиновых кислот; и (v) лизис стенок, вызванный автолитическими ферментами. Таким образом, у бактерий происходит потеря структурной организации и целостности цитоплазматической мембраны, а также другие повреждающие эффекты для бактериальной клетки [13]. ЧАС споростатичны; они подавляют рост спор (развитие вегетативной клетки из проросшей споры), но не сами процессы прорастания (развитие от покоя до метаболически активного состояния), хотя и по неизвестному механизму [14]. Аналогичным образом, ЧАС не являются микобактерицидными, но обладают микобактериостатическим действием, хотя фактическое воздействие на микобактерии мало изучено [15].
Хотя в некоторых исследованиях отмечено повышение толерантности к ЧАС, доказательств, подтверждающих развитие устойчивости к ЧАС в настоящее время нет [16]. Использование ЧАС конкретного наименования имеет свои преимущества и недостатки для конкретной ситуации, то есть выбор того или иного ЧАС в составе средства определяется для конкретного патогена, и этот фактор имеет решающее значение.
Полигексаметиленгуанидина гидрохлорид (CAS# 57028-96-3) является дериватом гуанидина, свойства, эффективность и воздействие которого еще не полностью изучены. В соответствии с Директивой по биоцидным продуктам от 16 февраля 1998 года (Directive 98/8/EC), вещество входящее в этот класс веществ (PHMB), на основании трех исследований, проведенных во время обзора досье BPR, было классифицировано как канцероген Carc. cat. 2 + H351 (подозревается как причина рака), категория 3; R40 (ограниченное доказательство канцерогенности). С данным веществом связано ряд инцидентов, в том числе с летальным исходом в Республике Корея в 2006 – 2011 годах (запрещено к применению в Республике Корея в 2011 году) [17] [18]. В мае 2016 года компания Reckitt Benckiser признала, что её продукты, содержащие ПГМГ, вредны [19]. ПГМГ ранее использовался в виде водного раствора (200 — 5000) ppm для дезинфекции кожи и инструментов. С 1 февраля 2013 года Европейская комиссия запретила использование ПГМГ в странах Европейского Союза во всех его ранее разрешенных областях применения. Европейская комиссия запретила размещение на рынке и использование ПГМГ для всех биоцидных целей [20].
Исходя из химического профиля данного соединения можно утверждать, что ПГМГ не является веществом, улучающим состояние кожи, использование его для таких целей неизвестно. Европейское химическое агентство (ECHA) своем сайте сообщает: «causes skin irritation, may cause an allergic skin reaction and may cause respiratory irritatio» (вызывает раздражение кожи, может вызывать аллергическую кожная реакция и может вызвать раздражение дыхательных путей) и «A majority of data submitters agree this substance is Skin sensitizing» (Большинство заявителей на регистрацию согласны с тем, что это вещество вызывает сенсибилизацию кожи) [21].
TETRANYL® U – продукт компании Kao Corporation, химическое наименование по INCI: метосульфат ундециленамидопропилтримония, CAS# 94313-91-4. Производителем [компанией КАО] этот продукт определяется как «Hair conditioning agent. It provides smoothness, shine and anti-static properties to the hair, making easy to comb it» (Агент для кондиционирования волос. Придает волосам гладкость, блеск и антистатические свойства, что облегчает их расчесывание) [22]. Данное соединение охарактеризовано AOEC (Ассоциация профессиональных и экологических клиник) как «A similar compound is a known human toxicant or allergen» (Подобное соединение является известным токсическим веществом или аллергеном для человека) [23]. В рецензируемой публикации сообщается, что соединение может вызывать репродуктивную токсичность у животных [24].
Глицерин, простейший представитель трёхатомных спиртов с формулой C3H5(OH)3, CAS# 56-81-5. Не токсичен, Европейское химическое агентство (ECHA) своем сайте сообщает: «According to the notifications provided by companies toECHA in REACH registrations no hazards have been classified» (Согласно уведомлениям, предоставленным компаниями в ECHA при регистрации REACH, опасности не были классифицированы) и «ECHA has no data from registration dossiers on theprecautionary measures for using this substance» (У ECHA нет данных из регистрационных досье о мерах предосторожности при использовании этого вещества) [25].
Глицерин обладает умеренным противомикробным и противовирусным действием и одобрен FDA [26] для лечения ран. Красный Крест сообщает, что 85 % раствор глицерина проявляет бактерицидные и противовирусные эффекты, а в ранах, обработанных глицерином, наблюдается уменьшение воспаления примерно через 2 часа. Благодаря этому он широко используется в продуктах для ухода за ранами, включая гидрогелевые листы для ожогов и другие средства ухода за ранами. Он одобрен для всех видов ухода за ранами, кроме ожогов третьей степени, и используется для упаковки донорской кожи, используемой в кожных трансплантатах [27]. Глицерин используется в медицинских, фармацевтических препаратах и средствах личной гигиены как увлажняющий кожу агент. Глицерин замедляет или предотвращает чрезмерное испарение спирта и воды с кожи, влияя на соотношение воды и спирта, которое, в свою очередь, влияет на антимикробную эффективность используемого средства.
Глицерин является наиболее эффективным увлажнителем по сравнению со многими другими веществами, в том числе a-гидроксикислотами, такими как молочная кислота и гликолевая кислота, гиалуроновая кислота, пропиленгликоль и бутиленгликоль, сорбитол, карбамид [28].
[1] Morton H. E. Alcohols. In: Bloch S. S., editor. Disinfection, sterilization, and preservation. 3rd ed. Philadelphia, Pa: Lea & Febiger; 1983. pp. 225–239
[2] Yasuda-Yasuki Y., Namiki-Kanie S., Hachisaka Y. Inhibition of germination of Bacillus subtilis spores by alcohols. In: Chambliss G., Vary J. C., editors. Spores VII. Washington, D.C: American Society for Microbiology; 1978. pp. 113–116.
[3] Bush L. E., Benson L. M., White J. H. Pig skin as a test substrate for evaluating topical antimicrobial activity. J. Clin. Microbiol. 1986;24:343–348.
[4] Coulthard C. E., Skyes G. Germicidal effect of alcohol. Pharm. J. 1936;137:79–81.
[5] Klein M., Deforest A. Principles of viral inactivation. In: Block S. S., editor. Disinfection, sterilization and preservation. 3rd ed. Philadelphia, Pa: Lea & Febiger; 1983. pp. 422–434.
[6] Larson E. L., Morton H. E. Alcohols. In: Block S. S., editor. Disinfection, sterilization, and preservation. 4th ed. Philadelphia, Pa: Lea & Febiger; 1991. pp. 191–203.
[7] Sykes G. The influence of germicides on the dehydrogenases of Bact. coli. 1. The succinic acid dehydrogenase of Bact. coli. J Hyg. 1939;39:463–469.
[8] Dagely S., Dawes E. A., Morrison G. A. Inhibition of growth of Aerobacter aerogenes: the mode of action of phenols, alcohols, acetone and ethyl acetate. J. Bacteriol. 1950;60:369–378.
[9] Man A., A. Ş. Gâz, Mare A. D., Berţa L. Effects of low-molecular weight alcohols on bacterial viability. Revista Română de Medicină de Laborator Vol. 25, Nr. 4, Octombrie, 2017
[10] Frier M. Derivatives of 4-amino-quinaldinium and 8-hydroxyquinoline. In: Hugo W B, editor. Inhibition and destruction of the microbial cell. London, England: Academic Press, Ltd.; 1971. pp. 107–120.
[11] Hugo W. B., Frier M. Mode of action of the antibacterial compound dequalinium acetate. Appl Microbiol. 1969;17:118–127.
[12] Salton M. R. J. Lytic agents, cell permeability and monolayer penetrability. J. Gen. Physiol. 1968;52:277S–252S
[13] Denyer S. P. Mechanisms of action of antibacterial biocides. Int Biodeterior Biodegrad. 1995;36:227–245.
[14] Russell A. D. Bacterial spores and chemical sporicidal agents. Clin. Microbiol. Rev. 1990;3:99–119.
[15] Russell A. D. Activity of biocides against mycobacteria. J. Appl. Bacteriol., Symp. Suppl. 1996;81:87S–101S.
[16] Gerba C. P. Quaternary Ammonium Biocides: Efficacy in Application. American Society for Microbiology Journals. 2015. Volume 81. Number 2. pp. 464 — 469
[17] Cummings K.J., Kreiss K. Occupational and environmental bronchiolar disorders. Semin. Respir. Crit. Care Med. 2015 Jun;36(3):366-78. Epub 2015 May 29.
[18] Dirk W. Lachenmeier. Chapter 24 – Antiseptic Drugs and Disinfectants // Side Effects of Drugs Annual. — 2015. — Т. 37. — С. 273—279.
[19] https://www.bbc.com/news/world-asia-36185549
[20].http://www.tukes.fi/fi/Ajankohtaista/Tiedotteet/Kemikaalituotevalvonta/Rajoituksia-ja-kieltoja-eraille-desinfioiville-aineille/
[21] https://echa.europa.eu/substance-information/-/substanceinfo/100.218.333
[22] https://www.ulprospector.com/en/la/PersonalCare/Detail/33232/996226/TETRANYL-U
[23] AOEC (Association of Occupational and Environmental Clinics) 2012. Asthmagen compilation — AEOC exposures codes.
[24] Melin V. E., Potineni H., Hunt Patricia, Griswold J., Siems B., Werre S. R. & Hrubec T. C. Exposure to common quaternary ammonium disinfectants decreases fertility in mice. 2014. Reproductive toxicology (Elmsford, N.Y.) 50, 163-170
[25] https://echa.europa.eu/substance-information/-/substanceinfo/100.000.263
[26] https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?fr=182.1320&SearchTerm=glycerin
[27] Stout Ed. I., McKessor A. Glycerin-Based Hydrogel for Infection Control. Adv Wound Care (New Rochelle). 2012 Feb; 1(1): 48–51.
[28] Sethi A., Kaur T., Malhotra S.K., Gambhir M.L. Moisturizers: The Slippery Road. Indian J. Dermatol. 2016 May-Jun; 61(3): 279–287.

В журнале «Управление финансовыми рисками» опубликована статья А. Полякова «Коммерческий кредит и его особенности применительно к бизнес-практике«. В статье рассматриваются характеристики коммерческого кредита как особой формы краткосрочного финансирования и специфика отношений поставщика и покупателя при использовании такой практики. Предлагается подход к оценке и снижению кредитного риска для поставщика.
Поляков А. Н. Коммерческий кредит и его особенности применительно к бизнес-практике // Управление финансовыми рисками. — 2020. — No4. — С.292–299.
перевод А. Н. Полякова






В статье рассматривается проблема влияния недетерминированных и неопределенных событий на методологию сценарного планирования, используемого при управлении рисками. Автор описывает методы управления рисками на основе интуитивной и обратной логики, показывает основные критерии инкорпорирования в сценарный анализ концепции антихрупкости, предложенной Н. Талебом.
Поляков А. Н. Антихрупкость как элемент методологии менеджмента риска // Управление финансовыми рисками. — 2020. — No3. — С.232–240.
Дезинфицирующие и антисептические средства относятся к специфической группе товаров, эффективность которых не может быть установлена потребителем непосредственно в процессе применения продукции по назначению. С учетом социальных рисков производство и оборот такой продукции должны находиться под особым вниманием как государственных регуляторов, так и соответствующих отраслевых объединений и ассоциаций.
Вспышка острой респираторной вирусной инфекции, вызванная вирусом SARS-Cov-2, выявила серьезные проблемы технического регулирования данной группы товаров на территории Таможенного союза. Так в условиях ажиотажного спроса на дезинфектанты и кожные антисептики начиная с весны 2020 года на рынке появилось множество продуктов, которые не соответствуют требованиям безопасности и целевой эффективности, предъявляемых к дезинфицирующим средствам. Наглядным примером отсутствия надлежащего технического регулирования является ситуация, когда регистрация дезинфицирующих средств для кожных покровов человека выполнялась под требования, установленные в Техническом регламенте Таможенного союза ТР ТС 009/2011 «О безопасности парфюмерно-косметической продукции», хотя этим документом не предусмотрена процедура испытаний целевой эффективности продукции, то есть установление в аккредитованной лаборатории наличия у продукта биоцидного действия (бактерицидного, вирулицидного, фунгицидного и т. п.) и его количественная оценка с выдачей соответствующего научного отчёта и экспертного заключения, и процедура проведения дезинфектологической экспертизы, служащие основанием для выдачи СГР; а также не определены критерии и показатели эффективности для продукции данного класса.
В результате потребитель фактически вводится в заблуждение относительно статуса и свойств продукции, регистрируемой по такой схеме. В такой ситуации следует обратить внимание на опыт стран Европейского Союза и США по регулированию производства и оборота дезинфицирующих средств.
В Европейском Союзе лишь та продукция может рассматривается как косметическая продукция, если маркировка, рекламные и информационные материалы не содержат никаких заявлений о её биоцидных свойствах, таких как: «антибактериальный», «антивирусный», «убивает 99,9 % микробов». Если на упаковке и в рекламе делается какое-либо заявление о биоцидном действии продукта, такой продукт попадает в сферу действия Регламента по биоцидным продуктам (BRP) (ЕС) 528/2012. Регистрация биоцидных продуктов в EC предусматривает две процедуры: требуется оценка и одобрение активного вещества (active substance) и авторизация биоцидных продуктов, содержащих активное вещество или их смесь, которые разделены на 22 типа (product-type, PT) в зависимости от области применения.
В США противомикробные препараты, предназначенные для использования на различных поверхностях, регулируются Агентством по охране окружающей среды США (US EPA) в соответствии с Федеральным законом об инсектицидах, фунгицидах и родентицидах (Federal Insecticide, Fungicide and Rodenticide Act, FIFRA). FIFRA требует одобрения конкретного продукта посредством процедуры регистрации антимикробных продуктов и их активных ингредиентов. Эффективность дезинфицирующего средства должна быть доказана лабораторными исследованиями, одобренными EPA.
Противомикробные препараты для использования на людях и животных регулируются другим федеральным агентством – FDA в соответствии с Федеральным законом о пищевых продуктах и косметике (Federal Food Drug and Cosmetics Act, FFDCA) по которому такие продукты считаются лекарственными средствами. Такие антисептические продукты, как дезинфицирующие средства для рук или салфетки для рук, регулируются FDA как безрецептурные лекарственные средства (over-the-counter (OTC) drugs). FDA в рамках своей программы монографий определяет признаны ли активные ингредиенты, используемые в безрецептурных препаратах, как безопасные и эффективные субстанции (generally recognised as safe and effective, Grase). В случаях, когда агентство устанавливает, что ингредиенты состава продукта не являются Grase, требуется регистрация такого продукта как нового лекарственного средства (new drug application, NDA). Соответственно, такие антисептические средства, как любые безрецептурные лекарственные средства, должны изготавливаться в соответствии с требованиями GMP (Надлежащая производственная практика), а производственное предприятие должно быть внесено в список FDA. Зарубежные предприятия, которые производят, переупаковывают или повторно маркируют лекарственные препараты для продажи в США, должны зарегистрироваться в FDA и зарегистрировать свои продукты в агентстве, и обязаны соблюдать требования CGMP (FDA’s current good manufacturing practices). FDA инспектирует предприятия по производству фармацевтической продукции по всему миру, включая предприятия по производству активных ингредиентов и готовой продукции. Если компания не соблюдает правила CGMP, любой препарат, который она производит, по американским законам считается фальсифицированным (adulterated). Хотя FDA формально не может заставить такую компанию отозвать продукцию, компании обычно отзывают её добровольно или по требованию FDA. Если компания всё же отказывается отзывать продукцию, FDA может оповестить общественность и конфисковать продукцию, обратившись в суд для вынесения постановления о конфискации или о судебном запрете при выявлении нарушении требований CGMP, даже если нет прямых доказательств несоответствий продукции, влияющих на эффективность конкретного препарата. Когда FDA возбуждает дело о конфискации, агентство просит суд вынести решение, позволяющее федеральным чиновникам изымать «фальсифицированные» продукты. В случаях когда FDA обращается за вынесением судебного запрета, агентство просит суд приказать компании прекратить нарушать CGMP. Как изъятия продукции, так и судебные запреты обычно приводят к вынесению судебных постановлений, которые требуют от компаний предпринять ряд шагов для исправления нарушений CGMP, которые могут включать ремонт помещений и оборудования, улучшение санитарно-гигиенических условий производства, выполнение дополнительных тестов проверки качества продукции и обеспечения обучения сотрудников. FDA имеет право возбуждать уголовные дела из-за нарушений CGMP, добиваться наложения штрафов и даже лишения свободы виновных лиц при определённых обстоятельствах.
Очевидно, что гарантировать эффективность и безопасность дезинфицирующих и антисептических средств путём предъявлений требований только к готовому продукту, а также путем анализа соответствия случайных выборок и образцов из партий (серий) продукции, невозможно, то есть регулирование отрасли должно включать и нормативные требования к производственным практикам предприятий, как это сделано, например, в США. Однако с учётом нынешнего состояния технического регулирования данной продукции на территории Таможенного союза необходимо начать разработку нормативных технических документов, определяющих требования к маркировке, упаковке, правилам приёмки и безопасности дезинфицирующих средств, а также определить критерии эффективности и методы оценки эффективности дезинфицирующих свойств.
В журнале Management #1 (53) 2020 (стр. 58 — 67) опубликована статья А. Н. Полякова «От кнута и пряника к самодетерминации. Краткая история мотивации«.




Директор СООО «Нобель Групп» Антон Поляков и руководитель отдела продаж Маргарита Петровская приняли участие в конференции «Менять мышление в системах управления с новыми стандартами ISO 9001:2015, ISO 14001:2015, ISO 22000:2018, ISO 31000:2018, ISO 37001:2016, ISO 45001:2018 и ISO 50001:2018”, организованной CERT Academy. Москва, 16 марта 2020 г.