Хотя оксиды аминов были известны химикам и изучались ими до 1900 года, но только после того как компания I.G.Farbenindustrie в 1939 году получила патент на такое вещество как диметилдодецил амин оксид, оксиды аминов были общепризнаны поверхностно-активными веществами. Через 22 года была выявлена полезность включения оксидов амина в рецептуры жидких средств бытовой химии, это способствовало широкому интересу производителей к этому классу соединений. Замена традиционно использовавшихся алканоламидов жирных кислот в качестве пенообразователей в рецептурах средств для мытья посуды на оксид амина – это конкретный пример применения этого вещества, приведший к его популяризации. Соотношение между количеством вводимого в рецептуру оксида амина и получаемым эффектом компенсировало его более высокую стоимость.
Реакция между перекисью водорода и вторичными или первичными аминами не приводит к синтезу веществ, интересных с коммерческой точки зрения, зато реакция с третичными аминами дает возможность получать такие вещества, которые можно использовать не только в различных моющих средствах, но, и в жидких отбеливателях на основе гипохлорита натрия, и как антистатик в текстильном промышленности, в качестве стабилизатора пены при производстве резины, как катализаторы полимеризации при изготовлении пластиков, в качестве антикоррозионных составов, как диспергатор кальциевого мыла и антибактериальный агент в твердых дезодорантах, что обусловлено замечательной совместимостью с другими компонентами состава и проявляемым синергизмом. Оксиды амина получаются в результате экзотермической реакции второго порядка между перекисью водорода и третичными аминами, природа которых может быть алифатической, ароматической, гетероциклической, алициклической или их комбинацией. В распространенных оксидах амина предшествующее поверхностно-активное вещество обычно C12-C18 алкилдиметил амин.
Оксиды аминов относятся к особому классу поверхностно-активных веществ, классифицируемых как амфотерные ПАВ. Это связано с тем, что оксид амина является цвиттер-ионой молекулой, которая при изменении pH от низкой к высокой величине меняет свою природу с катионной на неионогенную.
Оксиды амина имеют низкий коэффициент биологического накопления, легко удаляются стандартными способами очистки сточных вод, биоразлогаемы под действием аэробных и анаэробных бактерий. Все оксиды амина имеют токсичность от низкой до умеренной.
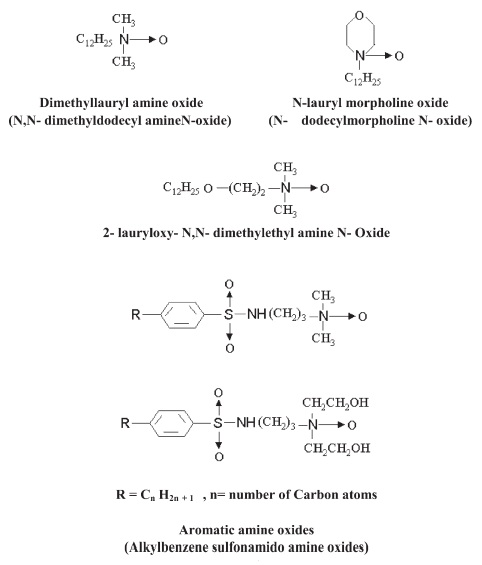
Синтез диметилалкил амин оксида и циклических амин оксидов
Диметиллаурил амин оксид, N-лаурилморфолин оксид, N-лаурилпиперидин оксид и N-лаурил-3-метил пиперидин оксид получали из соответствующих аминов путем взаимодействия с 51 % водным раствором перекиси водорода при температуре 75 °С. Скорость их синтеза указывает на то, что имеет место реакция второго порядка, и версии с пиперидином ситезируются медленнее, чем с диметиллаурил амин оксид, тогда как лаурилморфолин вступает в реакцию значительно быстрее.
Синтез 2-алкокси-N,N-диметилэтиламин N-оксидов
2-лаурилокси-N,N-диметилэтил амин N-оксид получали реакцией соответствующего амина с 30 % водным раствором перекиси водорода при комнатной температуре. Оксид амина концентрировали в сушильном шкафу при пониженном давлении и в результате получали кристаллический твердый оксид амина. Такие оксиды амина стабильны до температуры 100 °С, но быстро разлагаются до виниловых эфиров при температуре 150 °C. При низкой температуре имеет место деоксигенация оксидов амина до их третичных аминов. Гигроскопичность уменьшается по мере увеличения алкильной цепи.
Синтез оксидов амина на основе производных алкилбензола
Оксиды амина получали по трёхступенчатой схеме из ряда чистых 1-фенилалканов и смесевого детергента на основе алкилатов. Процесс включал (i) сульфирование фенилалканов с хлорсульфоновой кислотой в 1,2-дихлорэтане; (ii) реакцию полученного алкарилсульфонил хлорида с H2N(CH2)3NMe2, где Me это –CH3 группа, или с H2N(CH2)3N(CH2CH2OH)2, в безводных условиях при комнатной температуре; (iii) и окисление полученного третичного амина 30 % водным раствором перекиси водорода при 65 °С. Такой ароматический амин оксид был термически стабилен при температуре ниже 125 °С.